Czym działa gen HTR2B w walce z miażdżycą?
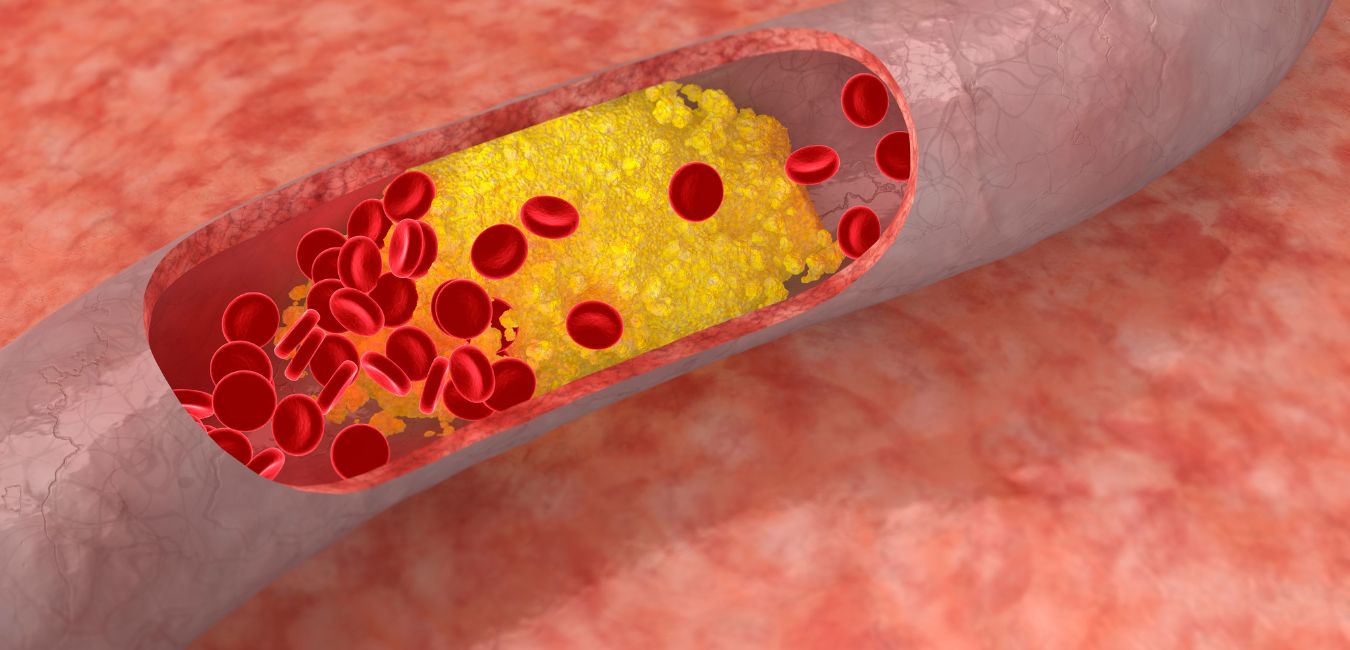
Miażdżyca to choroba, która dotyka miliony ludzi na świecie i może prowadzić do zawału serca czy udaru mózgu. Wyobraź sobie, że naczynia krwionośne to rurki, które przez chorobę zaczynają się zapychać i zwężać, utrudniając przepływ krwi. Naukowcy odkryli bardzo ciekawy mechanizm ochronny – gen HTR2B, który działa jak naturalny „strażnik” komórek naczyniowych. Chroni je przed szkodliwym procesem zwanym ferroptosis, który przypomina rdzewienie – tyle że „rdzewieje” wnętrze naszych naczyń przez nadmiar żelaza i szkodliwe tłuszcze.
W badaniach naukowcy testowali komórki naczyniowe wystawione na działanie utlenionego LDL – to jak zepsuty tłuszcz, który szkodzi komórkom (podobnie jak gdy jemy za dużo niezdrowego jedzenia). Okazało się, że gdy sztucznie zwiększyli ilość genu HTR2B w komórkach, te stały się znacznie bardziej odporne na uszkodzenia. Komórki z więcej HTR2B lepiej przeżywały, miały mniej szkodliwego żelaza i były w lepszym stanie ogólnym. Badania przeprowadzono też na myszach – te leczone aktywatorem HTR2B miały mniej blaszek miażdżycowych w naczyniach i lepiej zachowane komórki.
Najważniejsze odkrycie to zrozumienie, jak HTR2B chroni nasze naczynia. Gen ten włącza specjalny system alarmowy w komórce (szlak PI3K/AKT), który daje jej sygnał do obrony przed szkodliwymi czynnikami. To przełomowe odkrycie może zmienić sposób leczenia chorób serca – zamiast tylko leczyć skutki miażdżycy, moglibyśmy zapobiegać uszkodzeniom u samego źródła. W przyszłości można będzie opracować nowe leki, które będą naśladować działanie HTR2B i chronić naczynia krwionośne przed postępującymi uszkodzeniami, szczególnie u osób z wysokim ryzykiem chorób sercowo-naczyniowych.
Podsumowanie
Naukowcy odkryli, że gen HTR2B pełni rolę naturalnego ochronnika naczyń krwionośnych w walce z miażdżycą. Gen ten chroni komórki naczyniowe przed szkodliwym procesem ferroptosis, który można porównać do „rdzewienia” naczyń przez nadmiar żelaza i utlenione tłuszcze. Badania wykazały, że zwiększenie aktywności HTR2B sprawia, iż komórki stają się znacznie bardziej odporne na uszkodzenia wywołane przez utleniony LDL – szkodliwy tłuszcz podobny do tego powstającego przy niezdrowej diecie. Eksperymenty na myszach potwierdziły skuteczność tego mechanizmu, pokazując zmniejszenie ilości blaszek miażdżycowych w naczyniach. Gen HTR2B działa poprzez aktywację systemu alarmowego w komórce, uruchamiając szlak PI3K/AKT, który sygnalizuje komórkom konieczność obrony przed czynnikami uszkadzającymi. To odkrycie otwiera nowe możliwości terapeutyczne – zamiast jedynie leczenia skutków miażdżycy, medycyna mogłaby zapobiegać uszkodzeniom naczyń u źródła. W przyszłości możliwe będzie opracowanie leków naśladujących działanie HTR2B, co szczególnie pomoże osobom z wysokim ryzykiem chorób sercowo-naczyniowych.